HIV
Virus humane imunodeficijencije (HIV) jest retrovirus koji uzrokuje stečeni sindrom imunodeficijencije (AIDS, stanje u ljudi pri kojem imunosni sustav počinje slabjeti dovodeći do po život opasnih oportunističkih infekcija).
| Virus humane imunodeficijencije | |
|---|---|
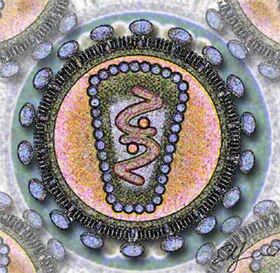 HIV | |
| Klasifikacija virusa | |
| Skupina virusa: | Riboviria |
| Carstvo: | Pararnavirae |
| Koljeno: | Artverviricota |
| Razred: | Revtraviricetes |
| Red: | Ortervirales |
| Porodica: | Retroviridae |
| Potporodica: | Orthoretrovirinae |
| Rod: | Lentivirus |
| Vrsta | |
| |
HIV je klasificiran u lentiviruse što je jedan od triju rodova retrovirusa. Karakteristično je za lentiviruse da su spori, što znači da se dugo zadržavaju u domaćinu koji polako napreduje u smrt. HIV ima samo 9749 nukleotida po čemu pripada među male viruse, ne samo u odnosu na ljudske stanice (koje imaju 3-3,5 milijarde nukleotida), nego i u odnosu na ostale viruse. Virus ima sferni oblik i sadrži dvostruki genom RNK-a. Kada uđe u stanicu domaćina virus rabi enzim reverznu transkriptazu da svoj genom RNK-a izmijeni u DNK, koji se zatim inkorporira u genom domaćina. Na taj način nastaje provirus.
Reverzna transkriptaza nema visok postotak točnosti tako da se mutacije događaju češće nego što je uobičajeno za prepisivanje DNK – RNK. Postoje dvije vrste (serotipa) virusa HIV-a: HIV1 i HIV2. HIV1 virus virulentniji je.
Virusi slični virusu HIV-a dosada su pronađeni kod mnogih primata što je dovelo do hipoteze da je riječ o istome prirodnom rezervoaru virusa.
Genom HIV-a
urediPostoji najmanje devet prepoznatljivih gena u sklopu genoma HIV-a, ali tri najveće strukture su GAG, POL i ENV i upravo njihova interakcija razlikuje HIV od ostalih poznatih retrovirusa.
GAG gen (group specific antigens) kodira virusnu nukleokapsidu, ovaj gen kodira sintezu virusu sličnih čestica kada ostala dva gena, POL i ENV, nisu prisutni. Gubitak funkcija GAG gena rezultira nemogućnošću HIV-a da “pupa” iz stanice domaćina. Zbog svoje važne funkcije GAG gen je okarakteriziran kao “stroj za stvaranje dijelova virusnih čestica”.
POL gen kodira HIV enzime kao što su proteaze, polimeraze, reverznu transkriptazu i integraze. Gubitak LTR u ovom genu zaustavlja virusni DNK splicing i onemogućava integraciju u stanični genom domaćina. Međutim, integracija virusnog DNK genoma u genom domaćina nije esencijalna za replikaciju virusa, zato što i neintegrirani DNK s nepotpunim LTR završecima još može proizvoditi nove viruse.
ENV gen kodira glikoprotein omotača virusa gp160 koji se enzimskim putem cijepa na gp120 i gp41. Ovi glikoproteini budu integrirani u staničnu membranu domaćina i postaju virusna ovojnica u procesu pupanja virusa i njegovog završnog procesa sazrijevanja.
LTR (long terminal repeats) duge terminalne ponavljajuće sekvence, koje se nalaze na krajevima virusnog genoma i imaju ulogu u usmjeravanju postojećih enzima stanice u kopiranju i vrše konverziju DNK integriranog provirusa u RNK.
Regulatorni geni
urediSljedeće strukture u okviru virusnog genoma koje je važno spomenuti su regulatorni geni. To su TAT, REV, NEF i VPU i drugi geni.
- TAT je trans-aktivatorski gen i on je jedan od prvih gena u okviru virusnog genoma koji će biti prepisan. Ovaj gen kodira trans-aktivatorski protein koji se koristi u procesu virusne replikacije.
- REV je regulator virusne proteinske ekspresije. Ovo znači da će on odlučiti hoće li virus sintetizirati više regulatornih proteina ili više virion komponenti. Vjeruje se da REV proteini kontroliraju razvoj infekcije od razdoblja mirovanja do razdoblja aktivnog rasta virusa.
- NEF je negativni regulatorni gen koji stvara proteine koji se zadržavaju u citoplazmi blizu nuklearne membrane. Vjeruje se da ovaj gen čini stanicu domaćina još više sposobnom za sintezu novih HIV viriona.
- VPU gen kodira protein koji utječe na oslobađanje novih virusnih partikula iz inficiranih stanica.
Ovi regulatorni geni imaju međusobnu interakciju na takav način da omogućuju virusu da se reproducira unutar stanice domaćina godinama bez opasnosti od smrti svog domaćina.
Replikacijski ciklus
urediNa površini plazmaleme svih živih stanica postoje složene glikoproteinske strukture koje nazivamo receptorima.
Postoje najmanje dvije vrste ovakvih receptora na površini T limfocita koji omogućavaju HIV virusu da se za njih pričvrsti. Prvi receptor važan za HIV je CD4 receptor na površini T-limfocita, a također je nađen na površini makrofaga i živčanih stanica. Drugi transmembranski receptor je esencijalan da bi došlo do infekcije. Dakle poslije vezivanja gp120 i CD4 dolazi do sljedeće veze nazvane koreceptorska veza. Koreceptor može biti jedan od mnogih membranskih proteina što zavisi od vrste stanice. Dva najčešća koreceptora su CXCR4 koji se normalno nalazi na površini CD4 T stanica i CCR5 koji se također nalazi na površini CD4 T limfocita, ali i na nekim makrofagima i dendritičkim stanicama. U normalnim uvjetima ova dva receptora omogućavaju stanicama imunosnog sustava da reagiraju na kemijske signale. U nekom slučajevima kada osobe imaju mutacije na ovim ko-receptorima virus nije u mogućnosti ostvariti puni spoj receptor-koreceptor, te ove stanice neće biti zaražene virusom. Da bi HIV inficirao stanicu T-limfocita neophodna su oba spoja receptor-antireceptor. Stanice kod kojih je ovaj transmembranski receptor drugačiji mogu izbjeći infekciju virusom jer antireceptor virusa ne odgovara izmijenjenom transmembranskom receptoru.
Tijesno pričvršćivanje virusnih čestica za receptore plazmaleme limfocita, omogućava fuziju virusa s plazmalemom limfocita.
Dva proteina gp120 i gp41 omogućavaju virusu da prepozna u koji tip stanice treba ući. Ovi proteini strše iz HIV omotača i služe kao antireceptori CD4 receptorima T limfocita.
Poslije ove faze ulaza virusa u stanicu, virusna RNK se reverzno komplementarno transkribira u DNK pomoću enzima reverzne transkriptaze. Bez ovog enzima genom HIV virusa ne bi bio u stanju da se inkorporira u genom domaćina te da se zatim reproducira.
Međutim upravo ovaj isti enzim ponekad pravi greške čitajući RNK sekvence, rezultat ovih pogreški je taj, da svi virusi sintetizirani unutar jedne stanice domaćina nisu identični. Ova različitost se ogleda u malim promjenama u molekularnoj građi njihovih ovojnica i enzima.
Sljedeća faza koja je karakteristična za replikacijski ciklus HIV virusa je faza integracije reverzno prepisane RNK sekvence u DNK. Za ovaj process integriranja virusnog DNK u DNK genom limfocita virus HIV posjeduje enzim integrazu. Ovako integriran virusni genom u genom domaćina nazivamo provirus.
Sve dok je ovaj limfocit u stanju mirovanja ništa se ne događa ni s provirusom, ali kada se limfocit aktivira započinje i transkripcija virusne DNK u mnogobrojne kopije virusne RNK. Sada ova virusna RNK postaje kôd za sintezu virusnih proteina i enzima i kasnije će biti uključena u obliku novih HIV virusa.
Sljedeća faza karakteristična za replikacijski ciklus HIV-a je faza translacije. U RNK genomu HIV-a postoji 9 gena. Ovi geni imaju kôd neophodan za sintezu proteina virusne ovojnice, kapside, transkriptaza, integraza i ključnog enzima proteaze.
Kada je izvršena translacija virusne RNK u polipeptidne sekvence one imaju oblik dugih lanaca koji su sačinjeni od nekoliko različitih proteina (reverzne transkriptaze, proteaze, integraze). Prije nego ovi enzimi postanu aktivni, oni moraju biti isječeni iz dugog polipeptidnog lanca. Virusni enzim proteaza siječe dugi polipeptidni lanac na individualne enzimske komponente koje omogućavaju sintezu novih virusa. I konačno virusna RNK udružena s proteinima kapside se pakira i oslobađa s površine limfocita, uzimajući i dio limfocitne membrane koja sadrži površinske virusne proteine odnosno dio membrane stanice u kojoj su se razvijali. Ovi površinski proteini će se zatim povezati s receptorima drugih stanica imunosnog sustava uzrokujući tako konstantnu infekciju. Ovi novoproizvedeni virusi su često identični prvobitnom virusu od koga su nastali, ali u slučaju HIV-a ovi novi virusi pokazuju varijacije u molekularnoj strukturi površinskih i drugih proteina i enzima što jako otežava tretman.
Infekcija
urediPrema UNAIDS-ovom izvještaju o pandemiji AIDS-a za 2005. godinu, u svijetu živi više od 45 milijuna ljudi zaraženih HIV-om. Brzina kojom se virus umnožava i velika sposobnost mutacije glavni su razlozi što svjetska epidemija ne jenjava.
Akutna HIV infekcija prolazna je simptomatska bolest, koja često ostaje neprepoznata, a javlja se 2-4 tjedna nakon zaraze virusom. Znakovi i simptomi često su nespecifični, najčešće uz temperaturu, upalu ždrijela, osip, povećanje limfnih čvorova i glavobolju. Mogući su i simptomi zahvaćenosti bilo kojeg organskog sustava. Čest je nalaz smanjenog broja leukocita, trombocita i poremećaj jetrenih transaminaza. Od velike je važnosti ciljana anamneza te potvrda dijagnoze akutne infekcije određivanjem prisustva virusnih markera u krvi. Od trenutka zaraze, osoba postaje doživotni nositelj virusa i izvor zaraze.
Vrijeme od infekcije do pojave prvih antitijela najčešće je jedan do tri mjeseca, rjeđe do šest. Stanje infekcije HIV-om bez simptoma može potrajati sedam do deset godina do pojave simptoma AIDS-a, od kojih su najčešći gubitak tjelesne težine više od 10 posto od normalne, temperatura viša od 38°C koja traje više od mjesec dana, dugotrajna i neobjašnjiva dijareja, gljivična infekcija usne šupljine i recidivi herpesa. Moguće su promjene na perifernom i centralnom živčanom sustavu. Krvne pretrage pokazuju smanjen broj svih vrsta krvnih stanica i povišene imunoglobuline. Nastaju infekcije s uzročnicima koji u imunološki zdravih ljudi inače ne izazivaju bolest.
Sa suvremenom, visoko aktivnom antiretrovirusnom terapijom počinje se najčešće kad broj CD4 T limfocita padne ispod 300 u mm3 krvi. Cilj je liječenja produžiti fazu HIV infekcije u kojoj još nema simptoma i vrijeme preživljavanja. Terapija ima ozbiljnih nuspojava, a osnovni je nedostatak razvijanje otpornosti virusa, kad prestaje njihova učinkovitost.
Muškarci koji imaju spolne odnose s muškarcima (MSM) su visoko rizična skupina za obolijevanje od hepatitisa, Sindroma stečene imunodeficijencije (AIDS/ kopnica)[1] kao i sifilisa. U Hrvatskoj je 2007. provedeno istraživanje koje ukazuje na sljedeće: njih 4,5 posto bilo je zaraženo HIV-om, a 10,6 posto ispitanika bilo je pozitivno na sifilis, a gonoreja je identificirana kod 13,2 posto muškaraca.[2] Posebno je značajan rizik za zarazom HIV-om: Od 56 dijagnosticiranih HIV infekcija u prvih 10 mjeseci 2012. bio je u 50 slučaja vjerojatni put prijenosa homoseksualno/ biseksualni odnos, što čini 89,3 % (u 2011. 48 od 76). U 4 slučaja heteroseksualni odnos (u 2011. 23 od 76), 11 slučaju dijeljenje pribora za intravensko korištenje droga, te u jednom slučaju nije bilo moguće doznati put prijenosa. Ovo je porast u odnosu na ranije godine - u Hrvatskoj je od 53 slučaja dijagnosticirane HIV infekcije u 2009. godini, u 40 slučajeva vjerojatni put prijenosa je muški homoseksualni odnos (u 2008. 50 od 67).[3] Ukupno u periodu od 1985. do 2012. homo/bisex je vjerojatni put prijenosa u 54,4 % svih zaraženih HIV-om.[4]
Godišnja učestalost HIV infekcije kreće se u vrijednostima 12-17 na milijun stanovnika, što Hrvatsku i dalje svrstava u zemlje niske učestalosti HIV infekcije (57/1 milijun prosjek za zemlje EU/EEA u 2011.). Među zaraženima i dalje dominiraju muškarci (86 %). Najveći broj infekcija registrira se u dobnoj skupini od 25 do 44 godina.[5]
Načini prijenosa
uredi- Seksualni prijenos – virus HIV se prenosi nezaštićenim spolnim odnosom s partnerom koji je inficiran virusom. Virus se prenosi putem krvi, sperme i vaginalnog sekreta.
- Krv i derivati krvi – intravenski narkomani predstavljaju sljedeću veliku grupu zaraženih HIV virusom. Oboljeli od hemofilije također predstavljaju rizičnu grupu, koji se inficiraju kroz kontaminiran faktor VIII koagulacije.
- Vertikalni prijenos – postotak prijenosa virusa s majke na dijete je oko 15 % u Europi, pa do 50 % u Africi. Vertikalna transmisija se može dogoditi transplacentarno prije rođenja, perinatalno za vrijeme porođaja i postnatalno za vrijeme dojenja novorođenčeta. U Hrvatskoj je od 1985. godine do danas ukupno 12 djece HIV dobilo od svojih zaraženih majki. Ovaj mali rizik još je znatno smanjen s mogućnošću primjene preventivne terapije kod HIV pozitivnih trudnica i novorođenčadi.[5]
Cjepiva
urediRazvoj cjepiva protiv HIV-a prate mnoge poteškoće. Sposobnost brze mutacije HIV virusa je jedna od najvećih prepreka stvaranju cjepiva. Kako se infekcija širi, proteini HIV antigena se mijenjaju brže nego što celularni i humorani imunitet mogu odgovoriti na novi antigen. Iz ovog razloga cjepiva zasnovana na jednoj lozi HIV-a nemaju efekta. Iz ovog razloga većina je istraživača odustala od pokušaja da se proizvede ovakva vrsta cjepiva. Međutim, na površini HIV virusa postoje određeni dijelovi koji nisu u stanju mutirati, tako da bi antitijela proizvedena protiv ovih "konstantnih" dijelova virusa mogla djelovati na sve loze HIV-a.
Sljedeći faktor koji utječe na brzinu istraživanja na ovom polju je taj da cjepivo mora ispunjavati određene uvjete.
Mora biti sigurno, oralno primjenjivo, jednodozno, stabilno, jeftino, i davati dugotrajan imunitet i biti djelotvorno na sve loze HIV-a.
Postoji teorija da bi se mogao proizvesti HIV virus koji bi se razmnožavao tako sporo, da ne bi bio opasan, nego bi inducirao celularni i humoralni imuni odgovor. Međutim, ovdje postoji strah da bi kod nekih ljudi virus mogao ponovo postati virulentan. Ovo se naziva reverzija. Postoje i vektorska cjepiva koja bi koristila druge viruse za unos određenih HIV gena u stanice domaćina. Ovi geni bi producirali proteine koje kodiraju HIV geni, na koje bi imunosni sustav stvarao antitijela i citotoksične stanice, tako da bi bio spreman za susret s HIV-om. DNK cjepiva se sastoje u direktnom ubrizgavanju gena u stanice domaćina u nadi da će neke stanice «pokupiti» ove gene. Kod vektorskih i DNK cjepiva ne postoji opasnost od HIV virulencije jer bi se koristili samo određeni geni.
Izvori
uredi- ↑ Vijesti.net: Održan okrugli stol o hepatitisu
- ↑ Spolnu bolest ima trećina testiranih homoseksualaca Arhivirana inačica izvorne stranice od 12. prosinca 2013. (Wayback Machine). Jutarnji List 19.10.2007.
- ↑ Epidemiologija HIV infekcije i AIDS-a u Hrvatskoj. HZJZ, 31. ožujka 2010. Inačica izvorne stranice arhivirana 2. ožujka 2013. Pristupljeno 1. ožujka 2013. journal zahtijeva
|journal=(pomoć) - ↑ Tatjana Nemeth Blažić, HIV/AIDS u Hrvatskoj. Epidemiološki pregled. Liječničke novine 115 (15.12.2012) 59-60.
- ↑ a b http://www.hzjz.hr/epidemiologija/hiv.htm Arhivirana inačica izvorne stranice od 2. ožujka 2013. (Wayback Machine) Tatjana Nemeth Blažić, dr. med.,Voditelj Odsjeka za HIV/AIDS, Epidemiologija HIV infekcije i AIDS-a u Hrvatskoj, 28. studenoga 2012., (pristupljeno 1. ožujka 2013.)