Benzotriazol
| Benzotriazol | ||||||||
|---|---|---|---|---|---|---|---|---|
 | ||||||||
 | ||||||||
| IUPAC nomenklatura | ||||||||
| Ostala imena | 1H-Benzotriazol 1,2,3-benzotriazol BtaH | |||||||
| Identifikacijski brojevi | ||||||||
| CAS broj | 95-14-7 ✓ | |||||||
| RTECS broj | DM1225000 ✓ | |||||||
| EC broj | 202-394-1 ✓ | |||||||
| PubChem broj | 7220 ✓ | |||||||
| Osnovna svojstva | ||||||||
| Molarna masa | 119,13 g·mol−1 | |||||||
| Izgled | ||||||||
| Gustoća |
1,36g/mL | |||||||
| Talište | 373 K[1] 100 °C[1] | |||||||
| Vrelište | 623 K[1] 350 °C[1] | |||||||
| Topljivost u vodi |
20 g·l−1[1] | |||||||
| Struktura | ||||||||
| Sigurnosne upute | ||||||||
| ||||||||
| Međunarodni sustav mjernih jedinica primijenjen je gdje god je to bilo moguće. Ako nije drugačije naznačeno, upisane vrijednosti izmjerene su pri standardnim uvjetima. | ||||||||
| Portal:Kemija | ||||||||
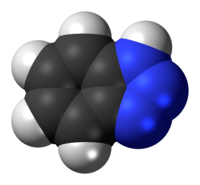
Benzotriazol (BTA) je heterociklički spoj koji sadrži tri atoma dušika, kemijska formula istog je C6H5N3. Ovaj je aromatski spoj bezbojan te polaran, te se može primjenjivati u razne svrhe.
Struktura
urediBenzotriazol predstavljaju 2 stopljena prstena. Njegov peteročlani prsten može opstojati u tautomerima A i B, a kao derivati oba tautomera javljaju se i strukture C i D.[2]
.
Sinteza
urediSinteza BTA uključuje reakciju o-fenilendiamina, natrijevog nitrita i octene kiseline. Konverzija ide preko dijazotizacije jedne od aminskih grupa.[3]
Primjena
urediKoristi se kao inhibitor korozije i to prije svega za bakar i njegove slitine, i to ne samo za industrijske primjene, rabi ga se i kod zaštite kulturnih dobara od spomenutih metala.Koristi se i u fotoemulzijama te pri analitičkoj determinaciji bakra, srebra i cinka.[2]
Utjecaj na okoliš
urediBenzotriazol je topiv u vodi, te nije lako razgradiv. Stoga ga se kod obrade otpadnih voda uklanja samo djelomice, te dio dospijeva i u rijeke i jezera.[4]
Pitanje kancerogenosti
urediPo propisima važećim u Europskoj uniji benzotriazol se deklarira kao tvar štetna za zdravlje. Ne preporučuje se neposredni kontakt s prahom, otopinama ili njegovim parama. Činjenica da nema opće prihvaćenih dokaza o njegovoj kancerogenosti ne znači da se radi o bezopasnoj tvari.[5][6]
Izvori
uredi- ↑ a b c d e 1H-Benzotriazole Arhivirana inačica izvorne stranice od 27. rujna 2007. (Wayback Machine), SRC PhysProp Database
- ↑ a b Sease, Catherine. Svibanj 1978. Benzotriazole: A Review for Conservators. Studies in Conservation. 2. 23: 76–85. JSTOR 1505798
- ↑ Robert A. Smiley “Phenylene- and Toluenediamines” in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim.
- ↑ W. Giger, C. Schaffner, HP. Kohler (2006): Benzotriazole and Tolyltriazole as Aquatic Contaminants. 1. Input and Occurrence in Rivers and Lakes. Environ. Sci. Technol. 40, 7186–7192. PMID 17180965
- ↑ http://www.bibra-information.co.uk/profile-294.html Arhivirana inačica izvorne stranice od 19. srpnja 2010. (Wayback Machine) Pristup stranici 27.08.2012.
- ↑ talasonline.com Arhivirana inačica izvorne stranice od 4. ožujka 2016. (Wayback Machine), pristupljeno 27. kolovoza 2012.
Dodatna literatura
urediSease, Catherine (May 1978). "Benzotriazole: A Review for Conservators". Studies in Conservation 23: 76–85.
Vanjske poveznice
uredi- Benzortiazole safety data Arhivirana inačica izvorne stranice od 4. ožujka 2016. (Wayback Machine)


